All aktivitet
-
studie om fosfatkinetik
Ni får den här också, en studie jag genomförde för ngr veckor sedan (som sedan ledde till en follow up) /JonasArticle_Phosphate_Binding_Kinetics vers2.PDF sammanfattning: This experiment is an attempt to investigate the dual mechanisms of phosphate binding to calcium carbonate surfaces within a marine environment. The experiment aims to differentiate between rapid, reversible surface adsorption and long-term, irreversible crystallization. I have posted my study/article as a pdf. Summary: The results demonstrate that while a significant portion of phosphate binds loosely and can desorb rapidly, approximately 57% of the total bound phosphate undergoes a slower transition into a stable, insoluble phase (likely hydroxyapatite), effectively permanently sequestering the phosphate within the calcareous matrix./Jonas Roman
-
2 nya studier jag gjort, sammanfattar i tråden
Hej Jag delar med mig av 2 nya studier jag genomfört. Dessa sammanfattar en del tankar jag haft sista tiden. Jag har skrivit dom på engelska, men sammanfattar ultrakort här: 1) Kalksten binder fosfat på 2 sätt. En lös bindning mellan kalcium o fosfat som inte är kristallin. Den har ganska hög löslighet. Sådan bindning sker inom 1-3 timmar. Går fram o tillbaka i enlighet med jämnvikt. Det andra sättet är hårda helt olösliga kristallina bindningar av calciumfosfat, sk hydroxapatit. Dessa tar dagar på sig att bildas och fosfat löser inte tillbaka ut i vattenkolumnen under normala akvarieförhållanden. En sten på 300 gram band 0.07 mg po4 på detta sätt i mitt försök, MEN jag är säker på att mer kan bindas, se artikel. 2) Fosfat som sänds in för fotometrisk analys, kommer alltid till viss del visa falskt lågt, då vattnet är biologiskt och därmed kommer fosfat i ngn utsträckning att förbrukas i röret. Filtrering med 0.22 um hjälper inte, men skjuter processen framför sig, där jag såg skillnad upp till 1 dygn, men därefter ingen skillnad i rören. Således bör provet filtreras, men trots det också analyseras inom ett dygn, ifall fotometrisk analys av PO4 på distans skall bli noggrann. Studierna är enkla att läsa och förstå. Detta är mina resultat, så det finns faktorer som kan göra att resultaten varierar. Håll till godo /Jonas A Study on the Rate of Phosphate Consumption in Water Samples (1).pdf How Much Phosphate Can a Phosphate (1).pdf
-
Sandbädden är vårt bästa biofilter.
Hej @ulfev Du kan addera ny sand till befintlig. Rör om lite så den blandas. Det har jag gjort många gånger. Ibland får man ju fylla på lite. I sumpen hade jag struntat i sand, det blir så liten area så det gör inte så mkt skillnad. Det som i mitt fall gjort skillnad denna gång är att jag i o med min öppna scape har så mkt fri sandyta. idag har det gått 2 år. Mitt po4 ligger på 0.06, nitrat 3. Och då har jag HÖG belastning med mkt fisk, och tillsätter ingen kolkälla. Inga tillsatser alls förrutom balling såklart. Mvh Jonas
-
Frisätter verkligen sten oorganiskt bundet fosfat?
Här kommer mer info: Detta vet vi/man: Fosfat kan bindas på 2 typsätt till kalkytor (läs kalksten, levande sten, sand): Dels en snabb bindning som är ganska lös, det är en sk bridging mellan Calciumjonerna på CaCO3 ytan och PO4 molekylen. Denna bindning är INTE en kristallbildning där kalciumfosfat bildas, utan en lösare, som dessutom sker snabbt. Oftast inom 30 minuter. Det är denna bindning som kan göra att PO4 går fram o tillbaka, dvs stenen "coatas" med Po4, men sedan släppa Po4 igen. Detta är en snabb effekt, alltså timmar, och enligt mig ganska ointressant, MEN kan förklara, och förklarar varför vi kan se hur PO4 direkt slukas upp vid dosering i kar med helt ny naken död sten. Samma mekanim ungefär som när nya CaCO3 ytor täcks med Mg. MEN, på lång sikt kommer en del fosfat, sakta men säkert bindas upp på det ANDRA typsättet till CaCO3 ytorna, nämligen i form av helt olösliga former av kalciumfosfat, tex hydroxyapatit., men det finns många varianter, samtliga mkt mkt svårlösliga. Denna process är långsammare, men kan alltså betraktas som icke reversibel, i alla fall inom normal temp och pH ej under 7, (egentligen kan pH gå mkt lägre utan att det löser upp sig men löslighetskonstanterna är definierade ofta vid temp 25 samt pH 7). När jag säger olösligt så är det sant i praktiken, men i teorin finns alltid en jämnvikt, MEN den är totalt försumbar, då vi pratar om löslighetskonstanter som är oändligt låga (10^-100 ish för vissa!!). Så, kristalliserat Calciumfosfat, inbyggt i CaCO3 etc, kommer aldrig att frisätta Po4 igen i ett akvarium. Så, skilj på den snabba omedelbara bindningen som är reversibel, och den långsiktiga. På sikt kommer ju alla akvarium med tiden mättas med de snabba bridgebidningarna (som kan fluxera fram o tillbaka), och mer o. mer binda upp PO4 långsiktigt istället "för evigt". Detta betyder att gammal sten som legat i hög Po4 behöver man enligt mig inte vara orolig för skall läcka tillbaka Po4. Vi pratar om död sten, Levande dito kan alltid frige po4 på grund av organiska ämnen, men det är nåt helt annat. Mitt test kommer bestå av en kort o en lång fas. Den korta är redan avslutad, den långa påbörjas nu. Vattnet har nu en po4 halt på 0.4 ppm. pH är buffrat upp till 8,6, ca 421, Mg 1313.Salthalt 35 PSI,Temp 21 ish. Efter 2 veckor tar jag upp stenen, sköljer av "restvatten", placerar den i rent saltvatten (ATI ref lösning) , mäter Po4 dagligen ngr dar. den snabba frisättningen om det finns kvar nån effekt av bridging, kommer direkt ge visst Po4 isåfall, men sedan är det sannolikt så att ingen ytterligare Po4 kommer friges. (min tes) Därefter kommer jag lägga stenen i HCL, och sen ,mäta Po4 igen, för att bevisa att stenen hade hårt bundet Po4 till sig överhuvudtaget, som alltså isåfall endast frisattes vid just mkt stark syrapåverkan (Saltsyra, 0.1 M). Jag sammanställer detta sedan. /Jonas
-
Frisätter verkligen sten oorganiskt bundet fosfat?
ja, jag skall förklara mitt upplägg nedan
-
Frisätter verkligen sten oorganiskt bundet fosfat?
Mitt svar är nej, jag har aldrig trott på att oorganiskt bundet fosfat frisätts från sten under normalt akvariepH. När vi ser att sten "frisätter" fosfat är det enligt min mening organisk ämnen som dör. Men det är nåt helt annat. Jag har inlett ett test idag, så får vi se om jag har rätt. Under tiden har jag sökt i litteraturen, och finner: Calciumfosfat, alltså den direkt bildningenmellan calcium och fosfat, finns i olika fomer men samtliga är extremt svårlösliga, läs olösliga i vatten. Dvs, har du väl en gång bundit fosfat till calcium till någon form av calciumfosfatförening, kommer inte fosfat att lösas tillbaka till vattnet så länge du inte lägger stenen i saltsyra...... Detta är fakta Men hur är det då med rena kalkytor, kalciumkarbonatytor? alltså sten. På dessa ytor binder fosfat, och JA, det stämmer att DEN bidningen är initialt inte en ren calciumfosfatkristallbildning, UTAN en ytbindning endast mellan Calcium och syret o fosfatjonen=denna bindning är svagare, och DEN bidningen skulle teoretiskt kunna gå tillbaka o frisätta fosfaten igen. MEN, denna bidning är kortvarig (tror jag) och övergår (vet jag) till så småningom bundet calciumfosfat, och DÅ är fosfaten där för evigt bunden. Det handlar om löslightskonstanten och den är för Ca+PO4=CAPO4 ((formeln är inte helt korrekt stochiometriskt) behäftad med en extremt låg löslighetskonstant. I folkmun helt olösligt, omätbar övergång till lösta ca o Po4 joner. Konstanten är i storlelskordningen upphöjt i minus9 till minus 29(för vissa former som tex hydroxyapatie). Vidare så har man visat att vid förekomst av fluor, som ju finns mkt av i ett akvarium, favoriseras denna inititala ytbidlning till den helt olösliga formen av hydroxapatit. Så kort sagt, kalksten kan suga upp Po4, men ej sen frisätta. Detta nyttjas ju i naturen, där vi kan se kalksten lite som GFO, en PO4 absorberare som mer eller mindre är en irreversibel process. Jag kommer idag starta ett försök, där jag tagit en bit sten, först kokat den så den är steril. Låtit den ligga en timma i Hcl så jag lakar ur all Po4 (för i Hcl går det). Sedan lägger jag den i en saltvattenslösning med PO4 0.2 ppm i ngr dar. Sen tar jag upp stenen, o lägger den i 100% rent saltvatten (ingen po4), och skall mäta Po4 efter ngr dar.Tesen är att vattnet kommer forsatt ha 0 i Po4. Återkommer med resultaten. https://www.sciencedirect.com/science/article/abs/pii/S0009254121003089
-
Romans Kalkylator
har precis lagt till S/sulfat till kalkylatorn. Fredrik kommer posta den så snart som möjligt. /Jonas
-
Kommande projekt Penninsula 500G2+
-
Kommande projekt Penninsula 500G2+
-
Kommande projekt Penninsula 500G2+
-
Ny ATI-balling
Låter mkt märkligt, och frågar du mig vill man aldrig ha organisk kolkälla i en Ballingbladning. Det vill man dosera separat och därmed ha full kontroll på. Du bör nog fråga ATI direkt, det måste väl finnas info på deras hemisda? Gå till källan så att säga:_)
-
Organo-MS - resultat och utvärdering
Jag kommer nog vara rätt så återhållsam med detta testet ett tag till. Ny informtion som vi inte vet hur vi skall hantera är inte alltid bra information. Vi kan jämflöra med sjukvården, vi undersöker alla med CT, vi ser massor av saker vi inte är intresserade av och som saknar relevens, MEN ställer nu ett krav på tolkaren som inte vet hur han skall hantera informationen. Med det följer oro, onödiga kontroller, samt kostnader. Parallellen är inte helt långsökt. Men säkert kommer en dag när vi vet mer vilka data som är intressanta, och hur vi skall tolka det, men fram tills dess kostar nog detta betydlig mer än det smakar, samt kan generara en del onödig oro samt fekaktiga slutsatser. Men, med det sagt, givetvis välkomnat med pionjärer, men var försiktiga med era tolkningar. Priset är ju högt (förståligt), och det kommer ta tid innan vi lärt oss om vi får ut ngt av det. /Jonas
-
Vad är det grumliga som bildas direkt när man häller sin basiska KH lösning?
Ja, de flesta KH blandningar idag består av Na2CO3, dvs inte NaHCO3, för att få en lösning som innehåller mer KH per liter. Skälet är 2, dels löser sig Na2CO3 lite mer än NaHCO3, dels bidrar en molekyl Na2CO3 med dubbelt så mkt KH som en molekyl NaHCO3. Så, nästan alla recept innehåller helt, eller delvis Na2CO3. Detta är till skillnad från NaHCO3, en mkt basisk lösning, vilket är skälet att det direkt blir en vit fällning i saltvattnet där KH lösningen droppas ner. Så, vilken kemisk förening är nu detta? Skälet att jag tar upp det är att en del tror o är rädda för att det är direkt bildat kalk, CaCO3, och därmed skulle ju en del av den tillförda N2CO3 bli poänglös för den förbrukas direkt. Svaret är Nej, det är (tack o lov) INTE CaCO3 som bildas, utan MgOH, och dessutom löser MgOH tillbaka så fort pH sjunker- Dvs inget av den KH du doserar slösas bort. Men varför bildas inte Ca CO3 da? Vi får ju jättehögt pH på en liten yta. Svaret är samma som varför det inte bildas CaCO3 när man gör ett calciumtest: Halten Ca och CO3 är helt enkelt för låg för att mättnad skall uppstå, SAMT reaktionen Ca-CO3=CaCO3 är långsam!, så det hinner inte bildas CaCO3 innan pH värdet är tillbaka igen på normala nivåer. Men med detta sagt, under extrema förållanden=väldigt hög dosering av Na2CO3 i ett område med dessutom svag cirkulation, då kan det teoretiskt vid sidan om MgOH faktiskt bildas lite CaCO3 också, men inte så mkt. Det är det vi kan se ibland vi väldigt höga Na2CO3 doser, att en del av den KH vi doserar blir inte tillgängligt för karet. Lösningen är fler doser, samt mer cirkulation i doseringsområdet. /Jonas
-
Varför är Magnesiumtester notoriskt svåra att få exakta?
Att titrera Calcium direkt är emkelt, man måste bara först maskera magnesium från lösningen, eftersom EDTA (det man titrerar med) är oselektivt , tar både Mg + Ca. Så, Mg maskeras enkelt genom att höja pH vätdet till 11-12, då bildas MgOH på sekunden, vitgrumligt. NU, kan du titrerar med EDTA och i o med att MG är maskerat, få ett selekterat Ca värde. Tvärtom då?, att designa ett Mg test, ja då måste man maskera Ca, och det går inte genom att bara höja pH, då maskeras ju Mg (MgOH). Så här måste man arbeta med att tillföra en selektiv ca bindare, och det finns ingen sådan som är 100% selektiv, utan det finns alltid risk att lite Mg binds också, eller att det binds för lite ca. Därför är ALLA Mg tester som titrerar ut Mg direkt, inte helt 100% exakta. Det finns ett sätt att lösa detta och designa ett Mg test som alltid är 100% exakt....det kommer jag berätta om en annan gång. Men nu vet ni varför det alltid är svårt med Mg tester. Red sea, colombo, salifert osv, använde lite olika calciumbindare, men alla dras med samma problem. Nu är det tack o lov inte så noga med Mg, så kan vi stå ut med +- 50 ppm, o det kan vi, så duger testerna. Men ändå, nu vet ni varför det ofta kan bli lite större variationer med Mg testerna ute i handeln. Jonas
-
Öppet hus Lördagen den 1/11-25
Tack för trevlig dag , samt möjligheten att få hålla en liten föresläsning
-
Test om mitt akvarium tenderar till att exportera CO2 till luften eller om det motsatta sker
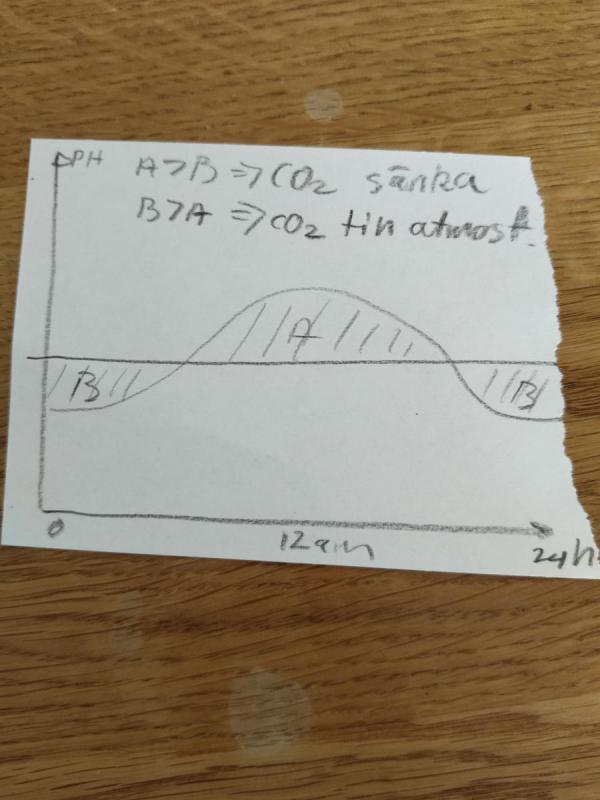
Exakt så. Det som kommer ha kanske den största avgörande betydelsen i ett enskilt fall om ett akvarium totalt sett (nettomässigt) blir en kolsänka (tar upp mer CO2 än avger) är ju luftens CO2. Givetvis en balans mellan detta och karets cellandning, men vad som blir nettoeffekten kommer bli olika i olika kar. a) Faktorer som bidrar till att karet kan bli en CO2 sänka totalt: Hög CO2 inomhus. Låg cellandning (inte så mkt fisk). Mkt alger b) Faktorer som bidrar till att karet bidrar till CO2 inomhus: Låg CO2 inomhus. Hög cellandning (mkt fisk). Lite alger Mitt kar gissar jag är enligt b, det avger mer Co2 än det tar upp totalt. Jag har hela den ljusa tiden ett pH över jämnviktspH eller mkt nära, och nattetid komme jag marginellt under. Om man gör en graf där man summerar arean som blir mellan jämnviktpH och aktuellt pH, så borde man på det sättet får reda på om karet är a eller b. I min skiss jag bifogar är jämnviktspH konstant (det raka strecket) men givetvis kan den linjen variera, det är bara att ta arean under oavsett. Oftast är det ju inte inomhusluften som varierar så mkt, som är orsaken till pH svängningar, utan fotosyntesen. Men som sagt, den matematiska modellen borde funka även om jämnviktspH (inomhusluftens CO2) ändras. /Jonas
-
Mastertronic Essential
precis detta har jag också fått fram. Kom ihåg viss osäkerhet i mätningarna. Jag gjorde exakt nu ett test med 2 mg/l nitrat, det gav en konverterings% på exakt 10%. så mellan 5-10% kan stämma, men snarast närmare 10%. Om detta är bra eller dåligt är inte frågan, det är upp till användaren att avgöra. Med en Hanna HR vid högt nitrit så är INTE nitrit oväsentligt , utan påverkar nitratvärdet väsentligt i falskt hög riktning. Det är fakta. Vid låga nitritvärden, normala, samt kanske ganska högt nitrat i karet, är det naturligtvis inget problem. Men vid omvänd situaiton, högt nitrit, lågt nitrat, kommer det spela roll vid tolkning av resultaten .
-
Mastertronic Essential
Som sagt, deras LR är i princip helt okänslig för nitrit, medans deras HR är inte det, där får man ta nitrit*10 och då får man falskt högt nitrat. Jag har verifierat detta flera ggr, senast precis nu, för att kunna bekräfta.
-
Mastertronic Essential
Det är som sagt en konverteringsfrekvens på 10% på Hanna HR, dvs om du har nitrit 0.5 mg/l i karet visar Hanna HR 5 mg/l nitrat för högt. Det är inte en fråga om bra eller dåligt, det så är det är designat, vilket är bra att veta i kar med högt nitrit. Senast hjälpte jag en person som visade sig ha 1 ppm nitrit i karet, dvs Hanna checkern HR visade 10 mg/l nitrat falskt högt. Det har betydelse i tolkningen. Däremot är deras LR mindre känslig, den konverterar över 100% (Liksom MTE.)
-
Mastertronic Essential
Inko Du var själv aktiv i den tråden....jag skall länka dig, men inte i denna tråd. Kan du inte öppna en tråd om ämnet så disk vi där?
-
Mastertronic Essential
Det stämmer inte helt som du skriver. Jag har också testat nyligen(i dagarna) och funnit annorlunda, att Hanna High range har en nitritkonverteringsgrad med cirka 5-10% (lite olika i olika range men ungefär, så i mitt fall när jag testade 10%), dvs om du har nitrit på 1 ppm, så visar Hanna HR 5-10 mg/l nitrat för högt. Low range Hanna verkar däremot (liksom MTE) konvertera 100% så där ger nitrit 1 mg/l endast falskt högt nitrat på 1 mg/l (som i MTE). Det är alltså skillnad här på HR och LR från Hanna (inte konstigt, LR tilltås reducera allt för att just få low range=högre färgkonstant, ungefär som vi gör i MTE). Det finns en tråd på annat forum där en person gjort ett mkt imponerande arbete med just Hanna HR och får fram samma resultat som jag. Salifert konverterar över 5%, och fauna marine 1%, så där om du har nitrit på 1 ppm, så blir det i salifert 20 ppm falskt högt nitrat, och i FM 100 ppm falskt högt nitrat. Vill påpeka att om vi skall fortsätta diskutera andra metoders nitritkänslighet, gör vi det gärna, men inte i denna tråd, då den handlar om MTE. Jämförelsen så här långt är relevant, men fortsatt eventuell disk om andra metoder uppmuntras men i annan tråd. /Jonas
-
Mastertronic Essential
Korrekt, den dimensionen skall det vara. Det är beklagligt att du inte fick rätt slang, samt i tid. Jag tvår mina händer, från min sida har jag gjort det som ska göras för att ordna detta i mkt mkt god tid, så det verkar va logistiken som inte klaffat. Där får jag hänvisa dig till FT eller Dejong. Men, ibland får man som du vara pragmatisk, så du gjorde du helt rätt som köpet slangen själv till slut. Men ja, var noga med dimensionen, 1.5-1.6 mm mm ID (cirka), den skall gå på ganska trögt när du trär på den. återigen, beklagar denna logistikmiss jag ej kunnat påverka, jag har verkligen från min sida stött på. Får du problem har jag en bit kvar jag kan skicka till dig gratis såklart. Har av dig isåfall /Jonas
-
Matning och fosfat
Att en mat är halvbra betyder jiu inte att fisken dör, maten är väl uppenbarligen tillräckligt bra. sen är det väl inte säkert att fisken behöver all den P som maten innehåller? kanske med andra ord inte är ett problem om fisken får i sig mindre P än vad maten från början innehöll? Oavsett så var detta intressant, och siffran ljuger ju inte. Jag har känt på mig detta länge men nu vet jag säkert, och kommer utnyttja detta för jag vill ju ha mer PO4 i mitt vatten. För säkerhets skull har jag alltid matat med pellets med och gör fortfarande, där jag har ju till skillnad från dig ngr fiskar som kanske är lite svårare?. Vitbröstad, Goldflake, Imperator, Navarchus, Bispinosus, naso, samt en del anthias (kanske inte så svåra), Midas, ocellaris, där i alla fall den vitbröstade, imperatorn o nason är rätt känsliga för ensidig mat. /Jonas
-
Matning och fosfat
Den ena kuben är större, angel formula. Så vikten stämmer rätt bra med det du angav.
-
Matning och fosfat
precis. Är det egentligen så konstigt? Kanske stora delar av cellerna är destruerade innan nedfrysning? Menar man inte att det faktiskt ÄR ensidig kost med bara fryst mat?