-
Antal inlägg
5 540 -
Gick med
-
Senaste besök
-
Dagar vunna
166
Typ av innehåll
Profiler
Forum
Kalender
Galleri
Saltvattensguiden.se ideell förening dokumentportal
Bloggar
Inlägg postat av jonasroman
-
-
On 2024-01-05 at 23:10, OR20 skrev:
Jag antar att det är till co2 scrubbern och inte dykutr. detta ska till?! Om du vill höja pH i karet varför använder du inte natriumhydroxid i din tre partslösning istället? Det borde ju ha en ”högre” pH effekt än receptet som det är nu. Det har ju funnits recept med det på nätet ett tag men du som är slipad på kemi har säkert någon tanke kring varför det inte är bra, förutom risken att hålla på med den typen av starka baser företås.
Sen skall nämnas att recepten vi har idag HAR en höjande pH effekt som inte är långt ifrån ren NaOH. Recepten består oftast av enbart Na2CO3 dom har ett pH på 12. Faktum är att vid stora doser blir detta ett problem då den tillfälliga o lokala pH höjningen gör att det precipiterar kalk och det går åt doseringslösning till annat än korallvöxt. Ett bekymmer med na2co3 baserade lösningar när dosen blir för hög. Lösningen är fler doser per dygn samt kraftigare cirkulation precis där man doserar. Detta fenomen talar också emot att använda NaOH.
-
 1
1
-
-
On 2024-01-05 at 23:10, OR20 skrev:
Jag antar att det är till co2 scrubbern och inte dykutr. detta ska till?! Om du vill höja pH i karet varför använder du inte natriumhydroxid i din tre partslösning istället? Det borde ju ha en ”högre” pH effekt än receptet som det är nu. Det har ju funnits recept med det på nätet ett tag men du som är slipad på kemi har säkert någon tanke kring varför det inte är bra, förutom risken att hålla på med den typen av starka baser företås.
Risken är att få obalans i det som bygger upp alkaliniteten. NaOH höjer alkaliniteten men inte då enbart CO3 alkaliniteten. Tanken med NaOH är ju att det högre pH drar ner co2 from luften och denna på grund av högre pH konverteras till karbonatet så indirekt får man karbonater. Men OH jonerna medför att alla andra alkalinitetsjonwe också ökar sitt bidrag till KH och risken blir att du med tiden får en alkaliniteten som inte byggs upp till 95% avd karbonater som vi ju vill. Vi tillsätter ju alkaliniteten i första hand som byggstenar för kalkbildning.
sen så finns risken med för högt pH o för snabba höjningar.
en co2 scrubber går direkt på grundorsaken, för högt CO2 i karet utan att tillföra en enda kemikalie till vattnet. Sen är det billigt också och teknisk extremt enkelt.
så jag väljer alla dar i veckan att separera problem och tillföra alk med karbonater och lösa pH problemet genom att dra bort co2.
jag är rätt säker på att ATI 2 part har delvis NaOH eftersom det ör omöjligt att konstruera en kh lösning som är 5 ggr strakare med bara karbonater. .
-
 1
1
-
-
-
-
-
On 2023-12-29 at 12:35, MichaelE skrev:
Fuktigare luft gör definitivt mediat mer effektivt, dock gjorde jag en habrovink där luften bubblade genom vatten längst ner i co2 scrubber när den inte var recirkulerande vilket borde ha lett till att luftfuktigheten var rätt hög redan då.
Min tanke är att med en recirkulerande design behöver bara scrubbern ta bort co2 som produceras i karet vilket har en övre begränsning i mängd pga att fiskar och andra biologiska procsswr bara kan generera en viss mängd koldioxid.
När man har en vanlig uppsättning så tar den först bort atmosfärisk co2 vilket finns i oändliga mängder.
Jag är dock öppen för att jag har lyckats med en tankevurpa. Det hade inte varit första gången.
E som sagt lit tveksam till den teorin. Skall fundera lite till även jag har tänkt fel förr :-)…men har en förklaringsmodell …återkommer ikväll

-
 1
1
-
-
45 minuter sedan, Christian J skrev:
Innebär det isf att samtliga ingredienser ackumuleras (jmf mina mätvärden nedan, inget Mangan)? Och hur löser man en sådan situation (förutom med stora vattenbyten), kommer ICP-tester att fortsätta visa för höga värden i all evighet trots att chaeton inte kan växa? Eller kommer de oavsiktligt komplexbundna ämnena att långsamt frigöras och bli tillgängliga med tiden?
Här är mina Triton-mätvärden för ChaetoGros ingredienser. Det verkar som om jag ligger högt över Tritons SetPoint för de här:
Ämne Mätvärde SetPoint ---------------------------- Iron 8 0 Molybdenum 48 12 Nickel 9 5 ...men nära SetPoint för de flesta övriga: Ämne Mätvärde SetPoint ---------------------------- Potassium 413 380-480 Boron 5 4.5 Manganese 0 0-3 Sulphur 911 900 Zinc 3 0-5Jag hade även för låga värden av Fluoride, Strontium, Iodine och Magnesium, men det kanske inte är relaterat till chaeto och ChaetoGro.
Du kan till att börja med exkludera alla joner som bara har 1+ , mycket svag affinitet till EDTA så där är jag helt säker på att du inte får någon konsumtion. Vi kan kika på affinitetsvärdet för olika jonerna men min gissning är spontant är att det inte har någon negativ effekt på några joner då det handlar om så oerhört små doser av EDTA.
-
 1
1
-
-
12 timmar sedan, Christian J skrev:
Tar inte phytoplankton också upp järn, som sedan hamnar i skummaren? Kan järntillskottet rentav öka tillväxten av phyto? Det är ju isf också en form av näringsexport.
ja det gör dom säkert, det är ju en alg.
-
2 timmar sedan, Claes_A skrev:
Haha, som SG förr... Kan bli blodigt...
Jag tror vi har samma förståelse. Problemet är att prata om kemiska jämvikter utan att prata om kemiska jämvikter... Det är ju sällan allt eller inget som talspråket kräver och hela tänket handlar om halter.
Jag tror så här:
Enstaka dos av Fe-EDTA fungerar säkert väldigt bra. En liten del av järnet blir biotillgängligt genom enkel kemisk jämvikt samt till del att andra joner med lika hög affinitet som järn hoppar in järnets ställe, alltså andra spårelemet (ej Ca2+ eller Mg2+). Jag är övertygad att att den låga halt räcker eftersom organiserna har system för att ta upp extremt låga halter av järn. Sen kan man fråga sig hur lång tid det tar i ett helt stort akvariesystem att nå kemisk jämvikt, alltså den där platån när som uppnås efter 4 h i grafen ovan. Eftersom Ca2+ ich Mg2+ gör kinetiken långsamt (de binder och släppår EDTA hela tiden så att det tar tid för EDTA att hitta Fe2+/Fe3+) så kan jag tänka mig att med akvariesystemets stora vattensystem, pumpar och de låga halterna av EDTA och järn som vi använder att det tar väldigt lång tid. D v s när väl en järnjon lämnar EDTA och diffunderar iväg så är vägen tillbaka en sak som tar sin lilla tid i den stora akvarievolymen.
När man sen doserar dag ut och dag in, eller vecka ut och vecka inså blir den - förvisso låga - EDTA-halten kanske ackumulerande. Man kan inte veta eftersom vi inte vet med vilken takt EDTA bryts ned i ett saltvattensakvarium. Går det t ex väldigt långsamt och man doserar rejält så byggs ju EDTA-halten upp. Och EDTA kommer nu att starkt komplexbinda inte bara järn utan även andra spårämnen: kobolt, mangan, nickel, zink - o s v. Deras biotillgänglighet minskar därmed jämfört med om att inte aggressivt doserat EDTA. Låter riskfyllt.
Och som du säger, ICPn kommer inte att ge något svar för den analysen berättar inte om jonerna är komplexbundna med EDTA.
Man kan ju tänka sig att detta är situationen hos @nike83 att järn nu förvisso finns biotillgängligt men att någon annan spårjon hindrar tillväxten av cheato p g a att EDTA komplexbinder den jonen. Mn2+ var ju en gissning.
klockren sammanfattning broder:-) Tänker exakt likadant, är med dig helt o hållet.
Frågan e således om man inte skulle nästa gång försöka hitta ett prep som är komplexbundet med citronsyra istället. Alternativt göra ett recept själv?
Gott nytt år
Jonas
-
 1
1
-
-
21 timmar sedan, Thomas Salt skrev:
Pråtede i dag med en i mine ögna dygtig, kynnig och nogran aquaist. Trods han är "ny" i branchen då har jag lärt mig massor av honom redan da han "nörder" sig inn i detaljer och vill förstå hur ting fungera.
Han hadde plötsligt fået problem med RTD trods hans kalkalger äntligen stortrivades, vi gik igennem ALT som var i princip perfekt, 7 månadar gammelt system, jag fatter intet.
30 min in i samtalet fik jag et hint... Cheato grow...
För typ 100 år sedan hadde jag stora problem med kalkalger som var invasive, @jonasroman tipsade om at jag hadde kansche högt Iodine, jag slutade dosera och problemet löste sig.
Han skal göre et IPC test i dag så skal bli interassant om dette är årsaken.
Men jag hadde aldrig haft en susning m det inte var för dette forum! Och dom som delar deras erfaring.
jag minns faktisk det nu när du nämner det:-)
-
 1
1
-
-
42 minuter sedan, Claes_A skrev:
Min ursprungliga poäng var ju just att EDTA läcker järn omedelbart som blir biotillgängligt och det visas i experimentet. Att det är 0,3% ändrar inte på det faktumet, det visar bara att EDTA har en hög affinitet för järn. Något som är välkänt.
Läser du studierna så finns också en ljuseffekt som påverkar hur järn frisätts från EDTA. Håller med om att det känns lite vanskligt att dosera EDTA i akvarium eftersom man inte vet hur länge det blir kvar och hur länge det binder upp olika ämnen. Det är ju inte bara järn som det har en hög affinitet för. Jag skulle nog välja att dosera t ex järncitrat.
Doserar man för mycket EDTA så får man ju biotillgänglighetsproblem med andra joner. Mangan, kobolt, nickel o s v.
Ja, då är vi överens, mitt inlägg handlade just om den oerhört starka bindningen, och det skrev jag som "respons" till ditt uttalande om att EDTA direkt läcker ut järn(kanske citerar dig lite fel). Dels för det ju inte alls är så direkt, o dels är det mikroskopiskt lite, och det var min poäng. Men då är egentligen på samma bana, pratade nog bara förbi varandra lite. Nu då till grundfrågan, denna extremt låga halt som EDTA släpper, räcker den? Vad är vitsen att dosera ett preparat som till 99.7% är obrukbart? Javisst, med tiden släpper EDTA alltihop, men det handlar ju om tid, och med den affiniteten kan det ta evigheter och processen är helt okontrollerad. Vi kanske får alldeles för lite fritt järn, i o med EDTAs enorma affinitet. För den tävlar knappt med tvåvärda joner då ju affiniteten är så mkt högre för järn 3+. Det finns ju andra sätt att binda med lägre affinitet, jag tror (men vet ej just nu ) att med citronsyra binds det svagare (som du också nämner)? Är detta skälet till att det kanske inte alltid funkar med järnprep? Och vad gäller ICP är jag nästan helt säker(men det kan vi ta reda på) på att EDTA bundet järn kommer med i analysen. I en ICP maskin upphättas ju provet till 10000 K och den mäter ju rena atomer oavsett dess "ursprung". Borde nog oxidera bort EDTAN?.
Läst om ljuseffekten, men det är väl mest UVljus? som vi inte har i våra lampor.
Så håller med dig, järncitrat är nog bättre. Läste just en artikel av Randy H om detta:-)
tack för givande diskussion, nu är SG som förr igen:-) haha
Jonas
-
 1
1
-
-
On 2023-12-29 at 15:40, Claes_A skrev:
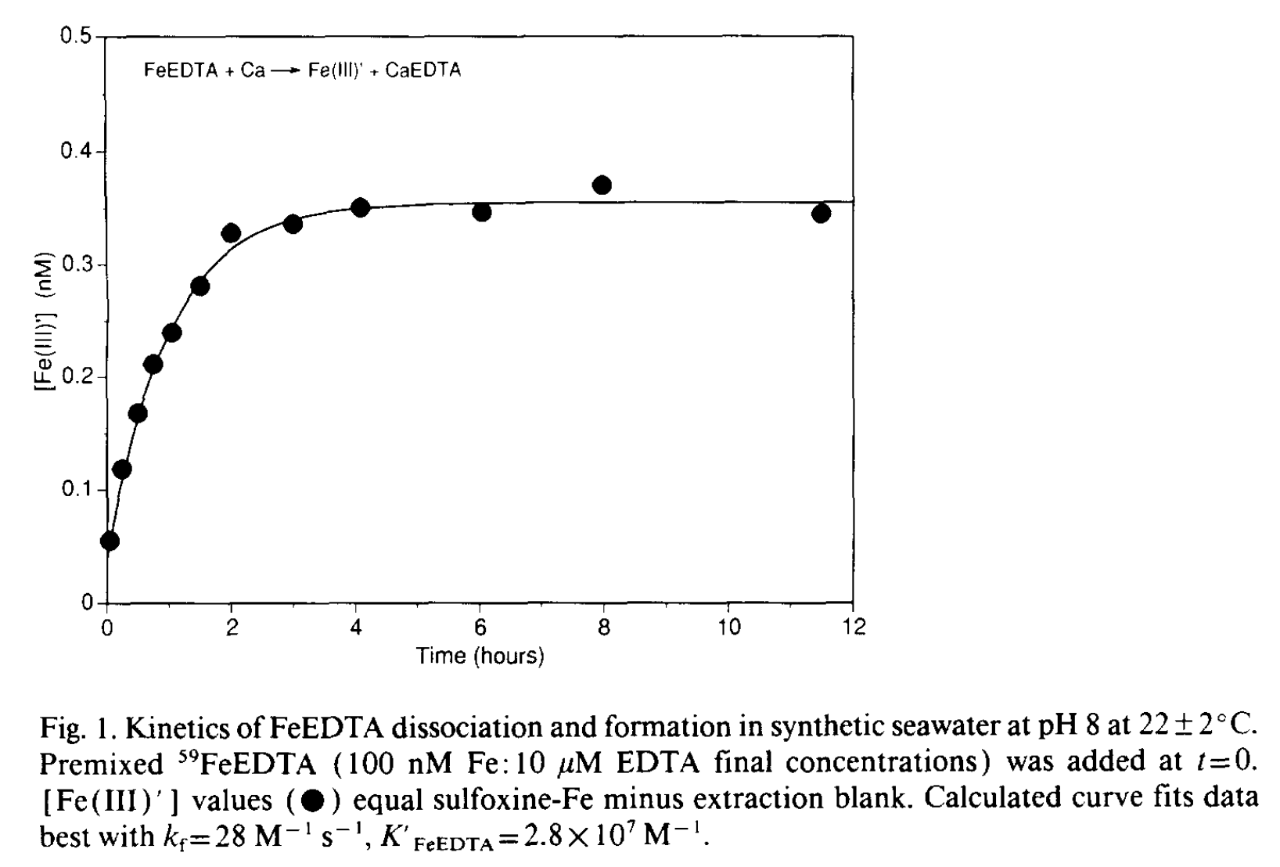
Jag var ju tvungen att kolla det här med Fe-EDTA i havsvatten. Tydligen är referensen för dessa mätningar Hudson, Couvault & Morel 1992, Marine Chemistry. 98:209-235. Dessa mätningar har sen reproducerats med annan teknik av Sunda & Huntsman 2003, Marine Chemistry 84:35-47.
Jag tycker figur 1 i Hudson-pappret är pedagogisk. Den visar hur radioaktivt Fe3+ komplexbundet av EDTA tillsätts till havsvatten och så följdes hur mycket som frigjordes från komplexet vid 100 nM Fe (5,58 mikrogram/L) och 100X överskott EDTA, alltså 10 mikroM. Det tar uppåt 4 h timmar att nå jämvikt (anges i texten bero på de höga halterna Ca2+ och Mg2+i havsvatten)
men kring 0,34 nM blir tillgängligt som fria järnjoner (som alltså är biotillgängliga) under dessa förhållanden. Koncentrationen järnjoner ligger i samma härad som IPC-testat som @nike83 har gjort. Där uppmättes 23,7 mikrogram/L nu i dec.
.
Båda studierna visar att Fe-EDTA komplexens stabilitet sjunker när pH ökar, kanske p g a att hydroxi-EDTA-komplex bildas: Ungefär 10X om man jämför t ex pH 7,8 och 8,3.
Lästips:
https://www.sciencedirect.com/science/article/abs/pii/S0304420303001014
https://www.sciencedirect.com/science/article/pii/0304420392900359
den bilden visar ju på det vi sagt tidigare, att det är en oerhört starkt bindning till EDTA. Av 100 nM frigörs bara 0.3%, dvs vi kan väl konstatera att EDTA-Järn är en mkt mkt stark bidning, under lång tid. Det hela bygger alltså på att EDTA frisätter så lite så det blir lagom för algerna. Måste va svårt o veta hur mkt mer EDTA bundet man måste tillsätta för att få lagom dos fritt, som dessutom sen mkt snabbt precipiterar. kanske därför som järntillsatser ibland inte funkar ?
-
 1
1
-
-
On 2023-12-29 at 14:20, Claes_A skrev:
Om EDTA-järn inte läckte järn rätt omedelbart så skulle det aldrig kunna vara biotillgänglligt. Eftersom vi vet att Fe-EDTA är biotillgängligt så vet vi rent empiriskt att komplexet läcker under akvarieförhållanden. Hur mycket och hur snabbt? Svårare fråga att svara på som alltid med kvantitativa frågor. Jag hittade någon artikel som pratar om en halveringstid på Fe3+-EDTA mätt på 20 dagar i flodvatten, alltså sötvatten. Mätning på havsvatten hade ju varit betydligt mer spännande för oss.
Hur det sen går till kan man fundera på. Säkert många processer på gång samtidigt. En faktor torde ju vara den enorma utspädningen när vi doserar Fe-EDTA. Under sådana förhållanden så när väl en järnjon har dissocierat från EDTA så blir möjligheten till återbindning under dessa mycket utspädda förhållanden extremt långsamma. Och det torde finns mängder av andra organiska molekyler i akvariet och inte minst celler som kommer att tar i järnet. Ljus anses ge reaktioner som bryter ned Fe-EDTA. Återigen så vet jag inte kinetiken.
-
För nu ganska många årsedan gjorde jag ett Ballingrecept som var 7 ggr starkare, ja motsvarande en triton core 7. För att göra det enkelt för er använde jag FM traces, och har räknat om så det passar mitt recept. Nu har FM justerat sitt Balling recept (eller troligen för ganska länge sedan) där deras KH dunk har en KH koncentration som är 1.8 ggr starkare än klassisk Balling (troligen har dom alltså adderat Na2CO3). Det betyder att mitt recept behöver justeras vad gäller traces 3 i KH dunken, och detta nedan är nu det rätta o inget annat för er som kör det recept jag kallar för "Romans Balling Forte Plus". Alltså ett recept på 4 dunkar som är ggr 7.
Många kör andra recept jag gjort som är ggr 3.5, samt på 2 dunkar. Där är det inga ändringar om jag inte säger nåt annat, men skall dubbelkolla alla recepten idag.
Romans Balling Forte Plus
(Balling Classic plus ggr 7)
Blandas upp till 1 liter lösning
Dunk 1
450 gram Calciumkloriddihydrat
5 ml fauna marines Trace-1
5 ml fauna marines Trace-2
Dunk 2:
128 gram Na2CO3
82 gram NaHCO3
9,7 ml fauna marines Trace-3
Dunk 3:
128 gram Na2CO3
82 gram NaHCO3
9,7 ml fauna marines Trace-3
Dunk 4:
69 gram Magnesiumkloridhexahydrat
170 gram NaCl-fritt salt
5.2 ml från dunk 2 och 5.2 ml från dunk 3 (10.4 ml av KH-lösningen) höjer alkaliniteten med 1.0 dKH i 100 liter vatten
Samma mängd (5.2ml) från dunk 1 höjer Calcium med 6.4 ppm
/Jonas Roman
-
-
2 timmar sedan, Claes_A skrev:
Det sker omedelbart eftersom Fe-EDTA läcker järn, dels genom jämvikt och dels för att andra joner kompeterar för komplexbindningen. Dessutom bryts Fe-EDTA ned av ljus och mikrober. Hur ofta dosera, en gång per dag eller en gång per vecka eller månad? Jag har ingen aning.
jag kollade upp, jag tror jag hade rätt. Affiniteten för Fe2+ är mkt högre än affiniteten för Ca och Mg som vi får anta är de kompetitiva jonerna. Om vi utrycker det i Log K(f) så betyder högre värde starkare bindning. Här är värdena för de joner vi pratar om:
Fe2+: 14,3
Fe3+: 25.1
Ca: 10,6
Mg: 8,7
envärdiga joner som Na, Cl osv har mkt mkt lägre affinitet o kan helt borstes ifrån därmed.
Så järnet ligger kvar bundet till EDTA när det kommer ner i saltvatten.
Ett exempel till, om du tar o titrerar Ca med EDTA så kommer färgen bli blå, om detta prov sen får stå, så förblir det blått i flera dagar, ja kanske för evigt. Det betyder att Ca med bindningsindex 10,6 EJ släpper EDTA. Då gör inte järn det heller som ju har ännu högre bidningsaffinitet. O testet ovan är utfört i saltvatten med kompetitiva joner.
/Jonas
-
2 timmar sedan, Claes_A skrev:
Det sker omedelbart eftersom Fe-EDTA läcker järn, dels genom jämvikt och dels för att andra joner kompeterar för komplexbindningen. Dessutom bryts Fe-EDTA ned av ljus och mikrober. Hur ofta dosera, en gång per dag eller en gång per vecka eller månad? Jag har ingen aning.
sen tror jag EDTA brytas ner mkt mkt långsamt så den biten är nog försumbar som orsak till att järnet du tillsatt blir obrukbart. Tror Stig pratade om månader. EDTA förvaras i ljusa flaskor, så det är nog inte så känsligt för ljus ändå. Mikrober tror jag inte bryter ner det så snabbt.
-
2 timmar sedan, Claes_A skrev:
Det sker omedelbart eftersom Fe-EDTA läcker järn, dels genom jämvikt och dels för att andra joner kompeterar för komplexbindningen. Dessutom bryts Fe-EDTA ned av ljus och mikrober. Hur ofta dosera, en gång per dag eller en gång per vecka eller månad? Jag har ingen aning.
Tror inte det stämmer. EDTA binder järn väldigt hårt, och EDTA släpper inte sina 2 värda joner så lätt, det är ju tex mekanismen bakom EDTA titrering.
-
23 timmar sedan, MichaelE skrev:
Det låter fullt rimligt. Däremot så borde man kunna sänka co2 halten i vattnet mer effektivt igenom att ha ett slutet system, det örnar min upplevelse. När jag tidigare körde med en ”vanlig” co2 scrubber låg jag på ett Max pH av ca 8.4, så fort jag började med min nuvarande lösning hoppade pH upp ett par punkter. Likaväl höll mediat ca 1.5 veckor och nu varar det över 4 månader. Jag har ifs ca 50% mer media i dagsläget men det är en rätt betydlig förändring.
Ja, det var något i den stilen jag ville minnas. Dock stämmer det säkert som du säger att det huvudsakligen är falska mätningar. Hur som haver så är jag mest intresserad av att förhindra att orp stiger för högt och det är det jag ser som värdet i att mäta redox.
precis, men beror inte det enbart på att luften du ni tillför är fuktigare? det medför att fler caOH2 molekyler i ditt media kommer till användning, och mediat rensar luften mer effektivt från CO2 men räcker också längre då det i praktiken är mer media som är aktivt. Har svårt att förstå om det skulle bero även på recirkulationen is ig, i min värld borde recirkulation ha motsatt effekt då den luften innehåller mer CO2 än rumsluften eftersom du tar luft precis när bubblorna mättats med akvariets överskott av CO2. Så jag skulle säga, trots recirkuleringen får du denna positiva effekt tack vare den fuktigare luften. Men jag kan ha missat nåt i min tanke, förklara isåfall gärna hur du tänker:-.)
-
-
1 timme sedan , MichaelE skrev:
Stämmer bra det. En pacific sun.
Min skummare stänger av när PH går över 8.5. Gör jag inget går den upp emot 8.7. Min probe visar rätt i referensvätska så förutsatt att inget stör ut den i karet så bör avläsningen vara korrekt. När jag lät pH gå upp över 8.6 såg jag lite utfällningar på pumpar osv. Jag skulle säga att PH snarare har gått upp i takt med förbrukning då jag tillsätter mer PH höjande baling.
Däremot kan det säkert även fälla ut lite med nuvarande värde.Gällande recirculerande design på co2 scrubbers så stämmer det helt klart att fuktigare media är mer effektivt, däremot tänker jag att en ytterligare effekt är det är faktiskt co2 i vattnet som tas bort ist för att man enbart förhindrar skummaren från att tillsätta co2 vilket också rimligtvis ökar effekten.
Nu är detta bortom min lekmannamässiga kunskap egentligen men jag har något som skramlar runt i bakhuvudet om att pH kan ha en direkt inverkan på redox-potential beroende på vad som ligger bakom den faktiska redox-potentialen…och i vissa fall kan det vara helt bortkopplat. Fick faktiskt lite huvudvärk när jag försökte komma ihåg hur det hänger ihop haha.
Gällande orp så håller jag med Signe stort. Det finns för mycket variabler som påverkar för att man ska kunna ha någon direkt nytta av det. Däremot så skulle jag inte köra ozon utan att ha en automatisk avstängning av enheten om det skulle sticka iväg.
Vad jag förstår så är den inte så pass avancerad så att den läser av den faktiskt koncentrationen av co2 utan när den släpper på co2 så minskar vattennivån något vid sensorn. När co2 minskar höja nivån igen och då släpper den på nytt.
Gällande mitt riktmärke så har jag inget. Min plan är att dra igång den och se vilka förutsättningar den funkar bäst under.
Absolut! Ska bli spännande, jag har inte använt en reaktor på väldigt länge så det lär bli en resa.
Kan vara så att det finns 2 skäl, dels att H jonerna påverkar o ger en falsk redoxstegring, alltså lågt pH=mer vätjoner=mer ström=falskt hög redox. MEN sen finns det en mekanism till som jag förstår det, med stigande pH så kan en del oxidationsmedel tappa lite av sin oxidationsförmåga (men får tillbaka den när pH sjunker), och då har vi en sann sänkning av redox faktiskt, som du skriver. Det kan ju tex ha o göra med att vissa oxidationsmedel är syra/baser och stiger pH så övergår dom i sin basiska form, som i sin tur kan ha en lägre oxidationspotential. Så är fallet för tex kaliumpermanganat, så teoretiskt kan det stämma. Dock tror jag då effekten är så tydlig att det mesta beror på störning av vätejonerna i redoxmätningen.
-
 1
1
-
-
53 minuter sedan, MichaelE skrev:
Stämmer bra det. En pacific sun.
Min skummare stänger av när PH går över 8.5. Gör jag inget går den upp emot 8.7. Min probe visar rätt i referensvätska så förutsatt att inget stör ut den i karet så bör avläsningen vara korrekt. När jag lät pH gå upp över 8.6 såg jag lite utfällningar på pumpar osv. Jag skulle säga att PH snarare har gått upp i takt med förbrukning då jag tillsätter mer PH höjande baling.
Däremot kan det säkert även fälla ut lite med nuvarande värde.Gällande recirculerande design på co2 scrubbers så stämmer det helt klart att fuktigare media är mer effektivt, däremot tänker jag att en ytterligare effekt är det är faktiskt co2 i vattnet som tas bort ist för att man enbart förhindrar skummaren från att tillsätta co2 vilket också rimligtvis ökar effekten.
Nu är detta bortom min lekmannamässiga kunskap egentligen men jag har något som skramlar runt i bakhuvudet om att pH kan ha en direkt inverkan på redox-potential beroende på vad som ligger bakom den faktiska redox-potentialen…och i vissa fall kan det vara helt bortkopplat. Fick faktiskt lite huvudvärk när jag försökte komma ihåg hur det hänger ihop haha.
Gällande orp så håller jag med Signe stort. Det finns för mycket variabler som påverkar för att man ska kunna ha någon direkt nytta av det. Däremot så skulle jag inte köra ozon utan att ha en automatisk avstängning av enheten om det skulle sticka iväg.
Vad jag förstår så är den inte så pass avancerad så att den läser av den faktiskt koncentrationen av co2 utan när den släpper på co2 så minskar vattennivån något vid sensorn. När co2 minskar höja nivån igen och då släpper den på nytt.
Gällande mitt riktmärke så har jag inget. Min plan är att dra igång den och se vilka förutsättningar den funkar bäst under.
Absolut! Ska bli spännande, jag har inte använt en reaktor på väldigt länge så det lär bli en resa.
håller inte med om tanken rörande CO2 skrubben. I samtliga fall så är det precis samma sak, skrubben tillför luft till skummare som är i princip helt fri från CO2. Mikrobubblorna i skummare har nu intitialt en CO2 halt på 0 ppm. Vatten luft interfacet, dvs kontakten mellan skummarvattnet o bubblorna kan liknas vid lungornas alveoler. Eftersom luftbubblorna innehåller 0 ppm CO2 och vattnet massor med CO2 , så kommer CO2 nu vandra från vattnet in i luftbubblan, och så kommer ske ända till bubblan innehåller lika mkt CO2 som vattnet, då stannar transporten, jämnvikt har uppnåtts o bubblan kan inte absorbera mer CO2. Bubblan som nu är maximalt mättad med CO2 (OCH har mer CO2 än rumsluften eftersom karets pH ligger under jämnviktsnivån) lämnar skummaren och den upptagna CO2 friges till luften, via skummarkoppsluften men givetvis snabbt även ut i rumsluften. Nu har vi på det sättet sugit ut CO2 från karets vatten. Om via istället tar luften via skummarkoppen blir det ingen skillnad därvidlag, luften som går igenom CO2 bädden o träder in i skummare kommer på samma sätt ha 0 ppm i CO2. Luften från skummarkoppen borde snarare ha lite mer CO2 än rumsluften då bubblorna lämnar sin CO2 via koppens luft, och på det sättet mättar mediat snabbare faktiskt!, MEN då luften är fuktig kan fler Ca(OH)2 molekyler användas och troligen väger det tyngre än den sämre skummarluften, så slutsumman blir att mediat räcker längre. Är inte säker på att mediat räcker längre i samtliga situationer, måste bero på sambandet mellan luftfuktighet och CO2 i rummet. kanske detta fenomen blir tydligare på vintern?
-
 1
1
-
-
40 minuter sedan, MichaelE skrev:
Stämmer bra det. En pacific sun.
Min skummare stänger av när PH går över 8.5. Gör jag inget går den upp emot 8.7. Min probe visar rätt i referensvätska så förutsatt att inget stör ut den i karet så bör avläsningen vara korrekt. När jag lät pH gå upp över 8.6 såg jag lite utfällningar på pumpar osv. Jag skulle säga att PH snarare har gått upp i takt med förbrukning då jag tillsätter mer PH höjande baling.
Däremot kan det säkert även fälla ut lite med nuvarande värde.Gällande recirculerande design på co2 scrubbers så stämmer det helt klart att fuktigare media är mer effektivt, däremot tänker jag att en ytterligare effekt är det är faktiskt co2 i vattnet som tas bort ist för att man enbart förhindrar skummaren från att tillsätta co2 vilket också rimligtvis ökar effekten.
Nu är detta bortom min lekmannamässiga kunskap egentligen men jag har något som skramlar runt i bakhuvudet om att pH kan ha en direkt inverkan på redox-potential beroende på vad som ligger bakom den faktiska redox-potentialen…och i vissa fall kan det vara helt bortkopplat. Fick faktiskt lite huvudvärk när jag försökte komma ihåg hur det hänger ihop haha.
Gällande orp så håller jag med Signe stort. Det finns för mycket variabler som påverkar för att man ska kunna ha någon direkt nytta av det. Däremot så skulle jag inte köra ozon utan att ha en automatisk avstängning av enheten om det skulle sticka iväg.
Vad jag förstår så är den inte så pass avancerad så att den läser av den faktiskt koncentrationen av co2 utan när den släpper på co2 så minskar vattennivån något vid sensorn. När co2 minskar höja nivån igen och då släpper den på nytt.
Gällande mitt riktmärke så har jag inget. Min plan är att dra igång den och se vilka förutsättningar den funkar bäst under.
Absolut! Ska bli spännande, jag har inte använt en reaktor på väldigt länge så det lär bli en resa.
just de ja, så var det den funkade. Ja du får se om den håller vad den lovar då:-)
-
 1
1
-
-
47 minuter sedan, Claes_A skrev:
Är det värt det? D v s är koldioxiden som kommer till akvariet via skummaren ett problem?
det beror på om du har ett CO2 överskottsproblem , dvs lågt pH problem eller inte. har du lågt pH beror det på för mkt CO2 i karet, och ofta i sin tur pgr av för mkt CO2 i rummet. Då löser man det med en CO2 scrubber.
-
 1
1
-












Kommande projekt Penninsula 500G2+
in 151-720 liter
Postat
precis så:-)