All aktivitet
-
Hjälp angående alger
fast på dessa bilder ser det ut som dino?---är dom tagna på samma plats? tidpunkt?. av ngn anledning är det ganska ovanligt med cyano o dino samtidigt, det ena brukar ersätta det andra. finns lite teorier om det.
-
Hjälp angående alger
Skulle säga cyano, här utan att ens tveka.
-
Hjälp angående alger
Håller med Lasse , att detta med kisel i vattnet skullar va orsaken vill jag påstå är en sällsynt orsak. För det första så har jag sett både dino, cyano och till o med kiselalger självt, vid LÅGT kisel, dvs under 100 ppb(enligt mina källor ligger kisel på cirka 100 ppb i NSW). Vid högt kisel, dvs över 100 ppb, har jag på motsvarande vis INTE sett mer ens av kiselalger. Min slutsats är: kiselnivån är oviktigt för uppkomst av cyano o dino, o tom av kiselalger...dvs vid normala halter av kisel bildas det alltid kiselalger på nya ytor. Jag tror det snarare handlar om konkurrens. Endast vid mkt höga halter av kisel i vattnet tror jag det blir ett problem, och isåfall blir det kiselalger o inget annat.
-
kontinuerlig KH-mätning...när kan vi köpa den prototyp som lär finnas?
Den här mojängen som nån snubbe i öst har själv byggt ihop som mäter KH kontinuerligt lär ha tillverkats i flera exemplar och testats ordentligt. Så var är den och varför får vi inte se den på marknaden eller tillgång till den? Har nån en kontakt? Rent tekniskt finns två sätt att mäta kh kontinuerligt på(finns fler så berätta för mig) Där jag är rätt säkert efter att ha sett bilder på apparaten att den tillämpar metod 2 Metod 1) man mäter pH och CO2(aq) kontinuerligt och då går det med en formel räkna ut KH då det finns ett matematiskt samband mellan kh/pH/co2(aq). Svagheten är att pH-mätningen måste va mkt exakt o kommer kräva en dyr elektrod o tät kalibrering. Metod 2) man surgör vattenprovet med tex saltsyra, ner till ett pH på 2. Då får man exakt alla karbonater att övergå till co2(aq). Därefter mäts co2(aq) (mäts kontinuerligt). Genom att ta detta mätvärde minus mätvärdet på co2(aq) innan surgörningen får vi mängden karbonater i vattnet innan surgörningen. Sen kan man med enkel matematik räkna om det till tex dKH. Denna metod är bättre tror jah för den kräver ingen pH-mätning utan enbart mätning av CO2(aq). CO2 i vatten mäts med en infraröd sensor och den är dyr. Resten är billiga saker. Sen krävs ju nån form av mekanisk lösning för att tillföra vattenprovet en viss mängd syra. Det ser ut på de bilder jag sett att så sker. Jag kan tänka mig att noggrannheten vid metod 1 är högst 0.5dkh o priset på en sån konstruktion borde bli närmare 10000kr. Det finns ingen marknad för det priset. Den andra metoden där hänger bara noggrannheten på CO2 mätningen. Kanske i slutändan vi där kan få en noggrannhet i bästa fall på 0.3dkh. Priset för den metoden är ju i princip co2 mätningen o med en serietillverkning kanske man får ner priset. Den kanske kan kosta i bästa fall halva priset mot den första metoden. Om den verkligen är såpass noggrann o co2 sensorn ej kräver alltför tät kalibrering så finns nog en grupp galningar som mig själv som skulle kunna lägga den summan för kontinuerlig kh mätning.
-
Ett nytt projekt
Lasse, kommer du dosera kolkälla ner i plenumet via plastslangen på bild? Vilket flödet har du ner i plenumet, alltså det flöde som är tänkt att gå upp ge om DSB´n? redoxmätningen....om vattnet står väldigt stilla i det röret...hur kan du vara säker på att detta redox representerar hela plenumets?...i tex en nitratreaktor har man en intern cirka pump på fler hundra liter i timman för att allt vatten i reaktorn skall ha samma redox...dvs om du styr din kolkälla med den redoxen som din elektrod i din setup ger, så kanske det blir en feldosering...jag tror du behöver mer bladning av plenumvattnet för att säkerställa en korrekt redoxmätning...men jag vet inte, bara en fundering.... vilka redoxvärden vill du ha i plenumet? kommer du styra kolkällan så du får det redox du vill ha? spännande setup...du är nog ganska först med denna variant...gillar den:-)
-
Ett nytt projekt
@Lasse, en kommentar: vad är egentligen vitsen med att krama ur ett filter o därmed återföra det organiska materialet i filtret till akvariet? då kan du väl lika gärna strunta i filtret helt så är detta organiska material hela tiden i karet o därmed matas korallerna hela tiden. Nu funkar ju bara ditt filter som en matsamlare, som du sen använder till att portionera ut maten vid olika tillfällen, den mat som ju innan redan fanns i karet. Sen om man vill mata ännu mer, så finns ju korallmat. Förstår inte, för ett filter skall ju antingen vara ostört för att fungera som ett biologiskt, dvs nitrifiering och/eller denitrifiering, eller ett mekaniskt o då kramas ur utanför karet,m dvs exportera icke nedbrutet organiskt material. En kombo av båda filtrena i två olika fysiska enheter är ju att föredra, men om man som du kör kombon i samma filter, dvs kramar ur ett mekaniskt filter tillbaka till karet, så kommer det ju inte fungera särskilt bra som vare sig mekaniskt eller biologiskt...mer som en ren korallmatare, och som sagt, för det finns ju bättre sätt. Dvs, tvek på den regimen Lasse;_)
-
Bästa valet för nitratreduktion?? - Svavelfilter, klassiskt nitratfilter eller "kombi"-filter/Aqua Medic
Du sammanfattar perfekt de olika filtrena och hur de fungerar:-) Du har rätt i att Aqua Medics variant med intern matning med deniballs har den svagheten att dosen av kolkälla blir ju konstant, och beroende av hur mkt deniballs man lade i från början. Men följer man deras rekommendation som är 2 liter deniballs i en NR1000-reaktor (o resten bioballs), så kommer reaktorn ungefär ha en kapacitet på 1.5 liter/timma. När vi talar om detta genomflöde så behöver det inte vara konstant, tvärtom, så fort redoxen blir för låg så måste och skall pumpen stanna så reaktorn hinner bygga upp en lägre redox, o sen startar pumpen igen osv. Det enda som är intressant är den totala genomströmningen, men om det sker i perioder om av och på spelar ingen roll, och är i princip alltså helt nödvändigt. Skälet är ju att annars skulle du aldrig kunna styra reaktorn för det är ju helt omöjligt att veta exakt vilket flöde den skall ha totalt...men genom att man ställer pumpen på tex 100% högre flöde än det man vill reaktorn maximalt skall prestera så har den lite marginal att stänga av och sätta på pumpen. Min pump ger just nu 2.5 liter /timma...om då reaktorn inte får ngn extern matning utan bara äter av dom interna deniballs, så kommer pumpen gå av o på i intervaller om cirka 10 min, dvs av 10 min, på 10 min osv...dvs effektivt flöde blir 1.25l/timma (=vilket stämmer bra med Aqua Medics specifikation av reaktorn). OM jag vill höja verkningsgraden så matar jag den bara dessutom med extern kolkälla...om jag gör det(2 gram per dygn) så går pumpen nästan på kontinuerlig drift då ju datorn styr den så redoxen ej går under -220mv...det ger ju en effektivitet på nästan 2.5liter/timma...alltså en dubbling av kapaciteten. Säkert kan man mata ännu mer o därmed öka flödet på pumpen osv. Ett riktmärke är att en nitratreaktor skall omsätta hela karets volym på 2-4 veckor. Vid hög belastning närmare 2-veckors gränsen, vid låg, närmare 4 v. Tex mitt system som är på 700 liter med hög belastning så behöver jag alltså krös igenom 700 liter på 2 veckor genom min reaktor, det kräver ett effektivt flöde genom reaktorn på 2l/timma...dvs om jag låter deniballs utgöra grunddoseringen samt stödmats med cirka 1 gram kolkälla externt per dag, så kommer jag ligga där ungefär. (testat mig fram till det). Jag tyckte det var en fördel med AM att det var just en grunddosering(deniballs)om man tex reser bort, dvs den lägger aldrig helt av...och om jag ser att mitt system samlar på sig nitrat trots detta, så kan jag ju bara gå in med extern stödmatning av reaktorn. MEN, i början måste du som du säkert vet mata den varje dag trots deniballs, i cirka 8 veckor. Där är jag nu ganska precis. Tror inte reaktorerna skiljer sig åt egentligen, man kan säkert köpa en deltec o lägga i deniballs tex(eller bygga en själv)...fördelen med dessa jämfört med de där påsarna som deltec pratar om, är ju att deniballs räcker i ett år!, dvs om den doseringen kolkälla som deniballs medför räcker för din nitratbelastning, så kommer du inte behöva öppna reaktorn eller göra nåt med den mer än en gång om året. Jag är mkt imponerad av att en sådan här nitratreaktor fungerar så bra. Mitt nitrat har på 7 veckor gått från 35 ppm till strax under 5 ppm...jag vill helst ner till 2.5:_) Jonas
-
Intryck efter DinoXal
Intryck efter Dinoxal:.Extremt effektivt, dinoflagelaterna försvann på 1-2 dagar. Men man ser ngr negativa effekter, vilket vore konstigt om man inte gjorde! Precis som för andra algmedel så påverkas givetvis inte bara exakt dinoflagelaterna (om inte detta är tex metronidazol vilket det anses ej vara då det ej skall påverka bakteriefloran), utan), utan de flesta encelliga algerna. Så det jag noterat är:Ingen algåterväxt på rutorna på en vecka, o generellt mindre eller inga mikroalger alls på andra inredningsdetaljer, pumpar osv. Till följd av detta har nitrat stigit, dels för att alger dör som då frisätter nitrat, men också pgr av minskad förmåga till återbildning av alger o därmed sämre förmåga för karet att ta upp nitrat av systemet förstås. Av samma skäl sker en liten pH sänkning då fotosyntesen minskar. Makroalger klarar sig men växer sämre. En del koraller ser lite blekare ut de som varit lite försvagade innan ser mest trötta ut, och ett litet vävnadsbortfall på en millepora. En lps dog, en favites, men den var kass från början men detta blev stötestenen som fällde den. Nu 10 dar snare o lite aktivt kol börjar färgerna mörkna lite igen, dvs korallernas zooxantheller börjar hämta sig. Man får ju inte glömma att zooxathellerna är en dinoflagelat men klarar sig hyffsat då den är skyddad...men ngt måste ju tas upp av korallen o hämma zooxanthellen lite.Jag har totalt sett vunnit på denna kur, men skulle bli bekymrad om jag tvingades inom kort köra en kur till...det tror jag inte är bra för karet. Förhoppningsvis slipper jag det. Får jag ett återfall längre fram o allt ser bra ut, tvekar jag inte att upprepa behandlingen. Men helt obemärkt har det inte gått förbi.
-
kamelräkor och SPS
Har nu ngr kamelräkor med ett stort antal sps:er....än så länge ser allt bra ut.
-
Läsa av Hanna checker "nyinköpt"
0.012ppm är i underkant o under det skall du absolut inte gå. jag tror dina koraller o hela karet kommer må lite bättre av att du höjer fosfat en smula, dvs helt enkelt slutar med fosfatremover o håller ett öga på fosfat. Under 0.02 bör man inte ligga.
-
Mitt 1800 liters revkar.
helt klart ibland det enda sättet:)
-
Kalibrera ATC-refraktometer
här är en länk där man testar ett antal hydrometrar från instant ocean där förutom en av dom visar spot on, likaså spot on från ett okänt fabrikat. Endast en hydrometer av billigt märke visade helt way off....jag har ägnat kvällen åt att söka runt...eftersom det tydligen finns två helt olika uppfattningar där båda lägren representeras av erfarna akvarister, så kan det inte ligga i annat än handhavandefel...hur skulle det annars kunna vara så olika uppfattningar bland akvarister med samma erfarenhet...i en tråd menar en akvarist som hållt i 40 år att hydrometrar är pålitliga, o i en annan tråd hävdas det omvända..alla har sin egna personliga erfarenhet som styrker...således borde inte problemet ligga i apparaturen utan hur vi handskas med den...jag kan inte få det till ngt annat...om vi bortser från enstaka outsiders som nåt mystiskt märke av undermålig kvalite...Jag kommer aldrig lämna min instant ocean, o till o med ,kontrollerar min refraktometer ibland med den o inte tvärtom....detta är ett kärt barn o återkommande ämne som vi kommer fortsätta att älta:-) http://www.advancedaquarist.com/2012/6/chemistry
-
Kalibrera ATC-refraktometer
diskussionen var på facebook Stig, med ett antal akvarister som kört med felaktiga värden en längre tid pga av refraktometerfelvisning...i samma tråd testade vi några svängarmshydrometrar av märket Instant ocean(ovetenskapligt förvisso), som visade samtliga exakt rätt, och refraktometern endast efter mkt noggrann kalibrering med batterivatten, ej med osmosvatten. En nära bekant hade nyligen mätt fel under en viss tid pga av felaktigt kalibrerad refraktometer osv osv. Jag säger inte att den visar fel om den är rätt kalibrerad, utan jag säger att just i o med att den kräver det så introduceras en osäkerhetsfaktor som inte en hydrometer är behäftad med. Beträffande känslighet o avlagringar så anser jag att det inte stämmer eller är så känsligt. Jag har mätt med instant ocean hydrometrar sedan 16 år tillbaka (eller mer, minns inte när dom började säljas), och vart ganska slarvigt med att skölja dom, faktiskt bara ibland sköljt i kranvatten, o alltid fått rätt värden, som jag då o då kontrollerat med tex en mkt noggrant kalibrerad refraktometer, o nu även med ett ATI-test. Refraktometern däremot kan jag aldrig få samma om jag inte är som sagt mkt noggrann med kalibrering( o ja, då visar den naturligtvis rätt)...därmed ser jag ju skillnaden i risk att det blir fel mellan dessa två sätt...där alltså båda funkar om man gör rätt.För grejen är ju just det...att göra rätt o sannolikheten för det. Och ja...jag har hört om kar som varit nära krasch för att man litat på en refraktometern och vid ett tillfälle pga av en dyr fin elektronisk salinitetsmätare(apex). Jag ser det så här...om du en gång testat din svängarm o vet att den mäter rätt, så se bara till att skölja den regelbundet, fyll den 2-3 ggr med akvarievatten vid varje mätning, undvik bubblor, håll den vågrätt...det kan inte misslyckas...har jag haft tur i 16 år?...fattar inte denna debatt som alltid drar igång kring svängarm...jag tror dina kunder slarvat.
-
Kalibrera ATC-refraktometer
o jag har sett flera som råkat ut för samma sak pga av felaktigt visande refraktometer..hmm... Jag tror det är handhavandefel i de fall man misslyckats med en svängarm, om vi nu exkluderar nåt enstaka märke som kanske är kasst, det låter jag va osagt. Sen detta med osmosvatten, jag har testat det gång på gång och får inte samma värde när jag kalibrerar med osmosvatten (trots nya filter mm) o batterivatten....o detta finns flera med mig som erfarit, vi hade en tråd på fb om det, där endast kalibrering med batterivatten fungerade för flera stycken. Jag såg en test på den svängarmsdito som jag har, och resultaten var mkt exakta(man tog 10 st tror jag). Instant ocean. Hur förklarar du rent teoretiskt att en svängarm kan visa fel? vad är felkällorna?...är den bara rätt konstruerad med rätt vikter osv från "fabrik", hur kan den då ändra sig, om vi förutsätter att den är ren o inte har saltpartiklar på svängarmen sållar??. Det får jag inte ihop. Däremot en refraktometer, har ju fler felkällor o behöver kalibreras o är väl beroende av kvalite på optik osv? Vattenmängden där är så liten så det räcker ju med minsta saltpartikel så blir det fel.
-
30 ppm nitrat, ingen fosfat
chaetomorpha har jag ju smitt refugium, men skulle väl vilja påstå att vid hög belastning o mkt högt nitrat så räcker det inte...däremot håller det nere min fosfat. Kväve tenderar ju att gå upp så mkt mer...o när vi då drar iväg upp emot 25-50 ppm osv...då får du odla väldigt mkt alger om du skall exportera det.
-
Kalibrera ATC-refraktometer
tvek på den;-)...kalibrerar man med osmosvatten o sen med tex batterivatten blir det sällan riktigt samma...osmosvatten är inte tillräckligt saltfritt för kalibrering anser jag. Tråden exemplifierar en sak jag tidigare tagit upp...refraktometerns svagheter och en vanlig svängarmshydrometer´s styrka...den förstnämnda är opålitlig om du inte är helt säker på att du kalibrerat rätt, o det kan va svårt att veta...en hydrometer, om du en gång får alla kontrollerat den mot en korrekt kalibrerad refraktometer, mäter alltid rätt. Jag använder aldrig min refraktometer längre, utan kör med min svängarmshydrometer som jag kontrollerat flera gånger o den mäter klockrent gång på gång (har även testat den emot ATI-test). Jag vet att det finns en del som anser att svängarmshydrometrar är kassa, men jag delar inte den uppfattningen baserat på min egen erfarenhet. Tänk på att svängarmshydrometern skall ligga i saltvatten i 24 timmar första gången, innan man kan lita på den, samt att det kanske finns fabrikat som är sämre o bättre.
-
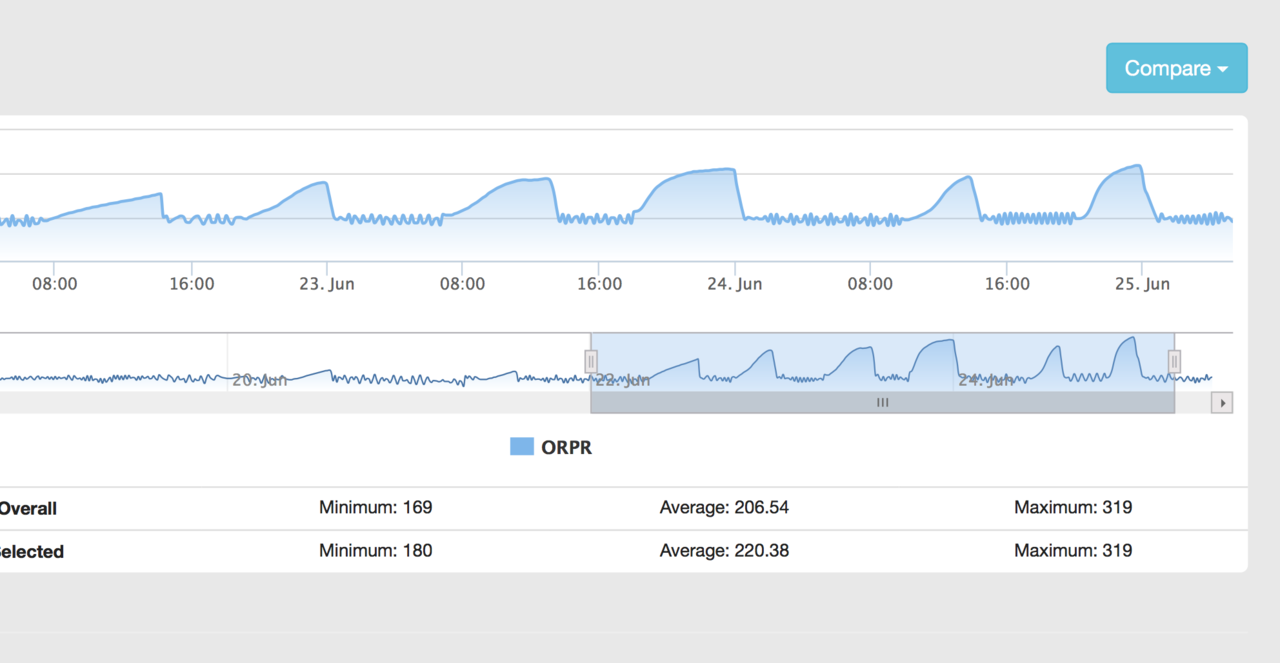
Uppföljning/uppdatering om min nitratreaktor.
Följande redoxmönster uppvisar nu reaktorn när den är mogen, dvs nån timma efter kolkälledosering sjunker redox ordentligt(tvärtom i tabellen, men tänk minus framför) o ligger kvar där i 3-6 timmar och doserpumpen går då alltså hela tiden i enlighet med programmet. Man kan väl likna det vid att hälla bensin på glödande kol o ett bevis på att reaktorn nu är ganska mogen o innehåller en ordentlig bakterierimassa, som svarar direkt på kolkälla. I början var kurvan mer rak oavsett dosering eller ej av kolkälla. Reaktorn går ju även på en intern dosering, i form av deniballs, som gör att kurvan om jag ej doserar externt tuggar på runt -200mv med doserpumpen då gående i "av och på" relation med cirka 10 min/10min...det gör att den totalt ger cirka 1.5 liter i timman, och vid extern kolkälledosering höjer jag den kapaciteten till nästan 3 liter i timman. Jag tänker dosera externt ett par veckor till, inte minst för att jag vill pressa ner nitrat lite lite till. Nitrat har stannat upp nu på 5 ppm i karet, kanske lite under...tror inte att reaktorn är överdimensionerad o kommer nolla nitrat, utan jag tror jag kommer kunna styra detta lite med kolkällan. Kör jag ingen kolkälla alls(dvs enbart deniballs för agera kolkälla), så gissar jag i detta läge att reaktorn blir ganska lagom för min belastning o kommer hålla mitt nitrat strax under 5...exakt vad jag ville. Men vi får se, men så tror jag utifrån de 7 veckor den nu varit ingång.
- Ett nytt projekt
-
Mäta kol i vattnet?
oki, tack för bra info:-)
-
Dinoxal
Uppdatering!: Efter två doser, alltså två kvällar i rad, var dinon borta till 100%!!...doserade en tredje dos för säkarhets skull dag 4. Ingen mer dosering planeras. Det står att man skall köra i tre dar extra, men jag stoppar lite tidigare då effekten var så otroligt god. detta medlet är ngt nytt...inga tidigare medel har fungerat så här snabbt o till 100%. Algenes funkar men tog minst en vecka, 10 dar...samt såg lite negativt på korallerna...undrar över dinoxal verkningsmekanism. Någon som vågar gissa? @Lasse, @stigigemla? Makroalger påverkas ej synligt. redoxen steg lite precis efter dosering men sjönk tillbaka sen. Skummaren skummade inte annorlunda eller mer än vanligt. Köpte medlet hos företagsakvarium.
-
kamelräkor och SPS
verkar som det ändå är värt att försöka då:-)
- kamelräkor och SPS
-
Mäta kol i vattnet?
@Dimorb, det var som jag trodde/gissade enligt ovan, att man mäter organiskt ämne i vattnet genom att oxidera detta o sen mäta CO2(aq). Lite mer exakt så gör man så här: man filtrerar vattnet med ett filter som är runt 0.2-0.7 ûm, det som då blir kvar är löst organiskt kol, DOC (det vi vill mäta). Detta vatten skall nu oxideras, eller rättare sagt , allt organiskt kol(DOC) skall oxideras till CO2. Det kan man göra på två sätt: 1) utsätta vattenprovet för hög värme , eller 2) UV-ljus ihop med ett oxiationsmedlet persulfat I båda fallen har nu DOC omvandlats till CO2(aq), där nu CO2 halten mäts (med ett instrument baserat på infrarött ljus). Innan man gör ovanstående oxidationer måste man omvandla allt oorganiskt kol, dvs karbonater, till CO2(vilket görs genom att sorgöra vattnet till pH 2.0...då går alla karbonater över som CO2(aq), o sen mäta CO2(aq)....det är sedan differensen mellan detta CO2(aq)-värde och det som man får efter oxidation av DOC, som blir ett mått på DOC-halten i vattnet. Att mäta CO2(aq) görs med en infraröd sensor. /Jonas
-
Mäta kol i vattnet?
dom erbjuder inte sådana mätningar
-
kamelräkor och SPS
Ja, vilken är nu eran erfarenhet egentligen av att kombinera kamelräkor (i syfte att hålla plattmask i schack), och sps. Vissa forum säger, NEJ!, dom äter sps, vissa säger ingen fara. Pär W har positiv erfarenhet av att det fungerar ihop med sps tex. Skall köpa ngr st i veckan, men vill höra om det finns fler än Pär som har erfarenhet. Mvh Jonas